Termodynamika opisuje związek między energią mechaniczną ciała a jego energią wewnętrzną oraz jej przekazywanie między ciałami.
1. O czym mówi nam temperatura ciała?
Jak już wiesz, cząsteczki ciał są w ciągłym ruchu. Oznacza to, że muszą mieć energię kinetyczną. Im większa jest energia kinetyczna ich ruchu postępowego, tym większą temperaturę ma ciało. Temperatura jest miarą średniej energii kinetycznej ruchu postępowego, przypadającej na jedną cząsteczkę substancji. Ponieważ cząsteczki są w ciągłym ruchu, czyli zawsze mają pewną, choćby bardzo małą, energię kinetyczną, temperatura zawsze musi być większa od zera. Na takim założeniu oparta jest bezwzględna skala temperatur.
2. Co to jest temperatura bezwzględna?
Temperaturą bezwzględną nazywamy temperaturę w skali Kelwina. Jest ona obrana tak, aby najniższa wartość była równa zeru. W tej skali nie ma wartości ujemnych. Zero w skali Kelwina nazywane jest zerem bezwzględnym lub też absolutnym. W tej temperaturze musiałby ustać wszelki ruch cząsteczek i dlatego temperatury żadnej substancji nie można obniżyć do zera bezwzględnego. Na co dzień używamy skali Celsjusza, w której za zero przyjęto temperaturę krzepnięcia wody (pod normalnym ciśnieniem).
3. Jaka jest zależność między temperaturą w skali Celsjusza i w skali Kelwina?
Temperatura w skali Kelwina (T) wiąże się z temperaturą w skali Celsjusza (t) następującą zależnością:
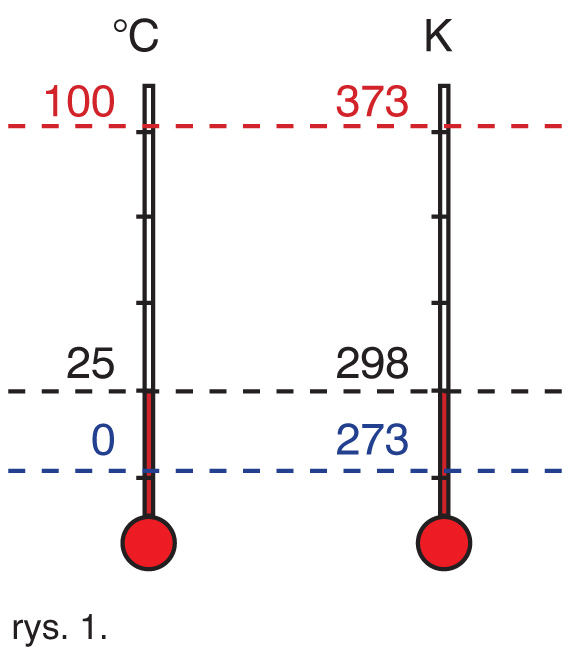
T = t + 273,15
Zależność obu skal przedstawia rys. 1.
4. Co to jest energia wewnętrzna?
Energia wewnętrzna (U) ciała to suma wszystkich rodzajów energii, jakie mają wszystkie cząsteczki tego ciała. Jest to więc ich energia kinetyczna ruchu postępowego, obrotowego, drgającego oraz energia potencjalna oddziaływań między cząsteczkami, energia wiązań chemicznych i energia jądrowa.
Z tych wszystkich rodzajów energii tylko ta część, która jest energią kinetyczną cząsteczek, może być wymieniona z otoczeniem.
5. Jak poznać, że energia wewnętrzna ulega zmianie?
O zmianach energii wewnętrznej informuje nas zmiana temperatury ciała. Temperatura zależy przecież od średniej energii kinetycznej cząsteczek. Jeśli temperatura ciała się zmienia, to znaczy, że zmienia się również średnia energia kinetyczna cząsteczek. A to oznacza zmianę energii wewnętrznej ciała.
6. W jaki sposób można zmienić energię wewnętrzną ciała?
Energię wewnętrzną ciała można zmienić na dwa sposoby: poprzez wykonanie pracy (W) lub przez przekazanie ciepła (Q) lub też obiema tymi drogami jednocześnie. Fakt ten zapisany jest równaniem jako pierwsza zasada termodynamiki:
Zmiana energii wewnętrznej ciała jest równa sumie wymienionego z otoczeniem ciepła (Q) i pracy wykonanej nad ciałem przez siłę zewnętrzną (W). Zapisujemy to równaniem:
Pierwsza zasada termodynamiki jest w gruncie rzeczy szczególnym zapisem zasady zachowania energii. Energia ciała zwiększy się zawsze o tyle, ile energii zostanie mu przekazane z otoczenia.
Pierwsza zasada termodynamiki jest w gruncie rzeczy szczególnym zapisem zasady zachowania energii. Energia ciała zwiększy się zawsze o tyle, ile energii zostanie mu przekazane z otoczenia.
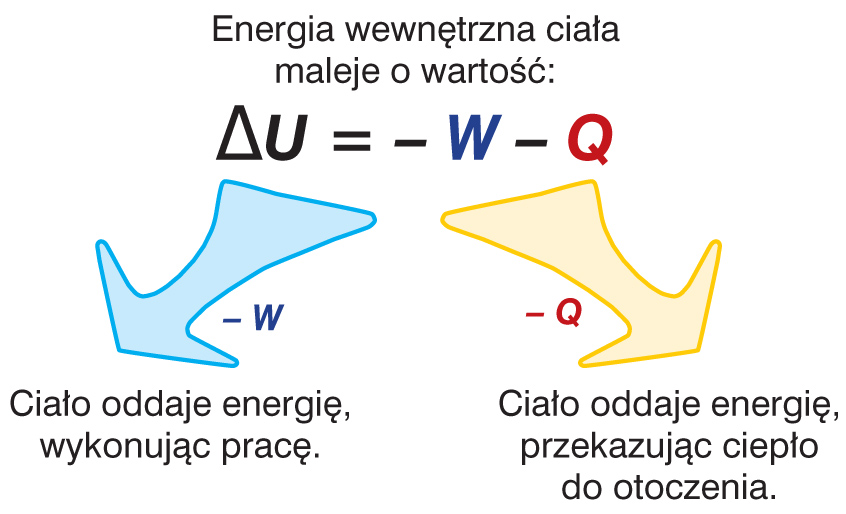
Ciało zmniejsza swoją energię dokładnie o tyle, ile energii przekaże do swojego otoczenia.
Skojarz na przykładzie!
Gdy wciskasz tłok pompki, działasz siłą skierowaną zgodnie z przesunięciem tłoka. Wykonujesz wówczas pracę nad powietrzem zawartym w pompce. Gdy ściskasz sprężynę, działasz siłą skierowaną zgodnie z przesunięciem końca sprężyny, czyli wykonujesz pracę. Podobnie gdy pocierasz łepek zapałki o draskę, wówczas również wykonujesz pracę nad ciałem. W każdym przypadku wykonana przez Ciebie praca zwiększa energię wewnętrzną ciała.
Gdy dotykasz gorącego kaloryfera, to przekazuje on Tobie energię w postaci ciepła. Gdy ogrzewasz wodę w czajniku elektrycznym, to grzałka przekazuje ciepło do wody. W obu przypadkach mamy wzrost energii wewnętrznej ciała.
7. Na czym polega proces izochoryczny?
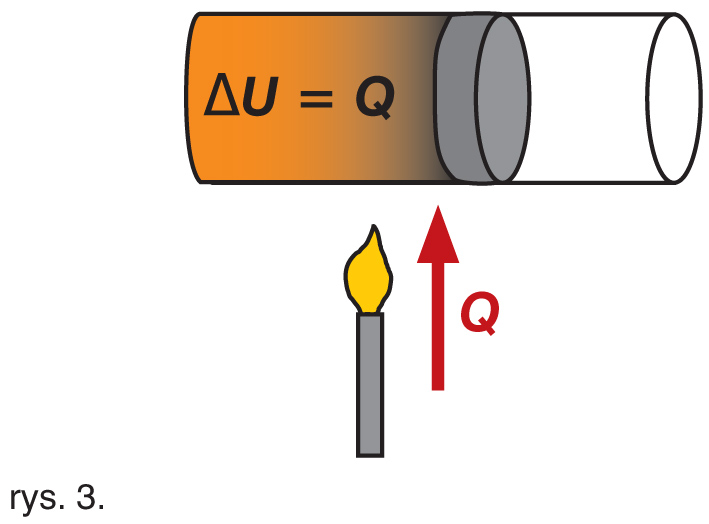
Jeśli gaz w zamkniętym zbiorniku zwiększa swoją energię wewnętrzną, ale nie może zmienić przy tym swojej objętości, to mówimy o przemianie izochorycznej. Najprostszym sposobem takiej przemiany jest ogrzewanie zamkniętego zbiornika z gazem, czyli doprowadzanie do niego energii pod postacią ciepła. Gaz zwiększa wówczas swoją temperaturę i ciśnienie, ponieważ drobiny intensywniej się poruszają i uderzają w ścianki zbiornika (rys. 3). W tym przypadku przyrost energii wewnętrznej gazu jest równy ciepłu pobranemu z otoczenia, czyli: ∆U = Q.
8. Na czym polega proces izotermiczny?
W tym procesie stała jest temperatura. Jest to możliwe, np. gdy wykonujemy pracę nad gazem, czyli go sprężamy, a gaz pobraną w ten sposób energię oddaje jednocześnie do otoczenia w postaci ciepła (rys. 4). Praca wykonana nad gazem jest dokładnie równa ciepłu oddawanemu do otoczenia i wówczas ∆U = const.
9. Na czym polega proces adiabatyczny?
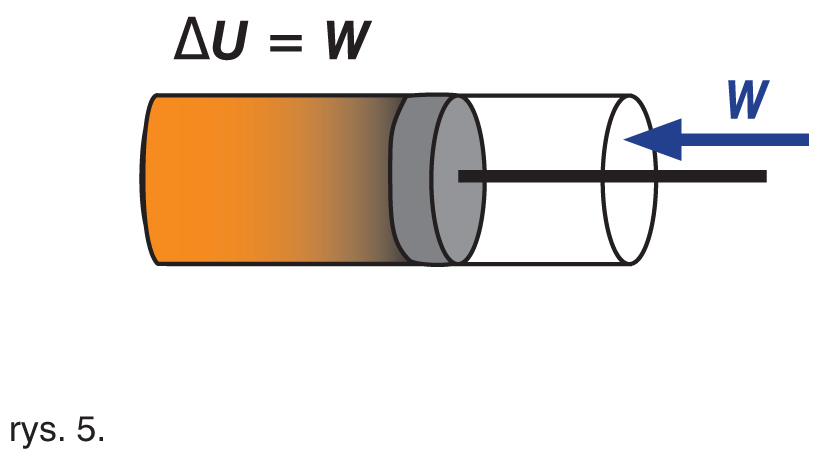
W tym procesie nie zachodzi wymiana ciepła z otoczeniem. Jeśli w takich warunkach wykonamy nad gazem pracę, to jego energia wewnętrzna wzrośnie dokładnie o wartość wykonanej pracy, czyli: ∆U = W (rys. 5).
10. Na czym polega proces izobaryczny?
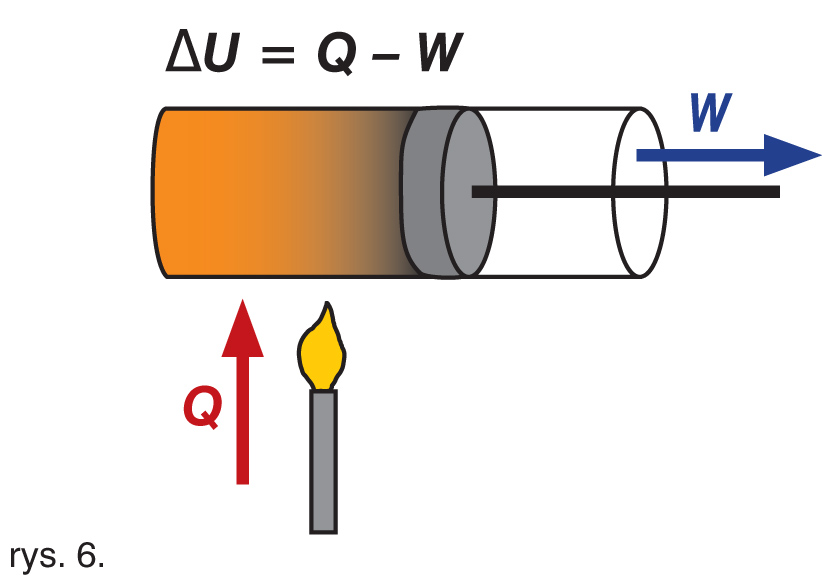
W tym procesie stałe pozostaje ciśnienie gazu w zbiorniku. Do gazu dostarczamy ciepło, rośnie jego temperatura i ciśnienie. Gaz wykonuje pracę kosztem części dostarczonego ciepła (rys. 6). Reszta ciepła powoduje wzrost energii wewnętrznej gazu, czyli: ∆U = Q – W.